Pengertian Ikatan Hidrogen: Senyawa, Contoh Soal - Hello adik-adik yang baik, bertemu lagi dengan Bospedia. Kali ini kita akan membahas tentang ikatan hidrogen. Ikatan hidrogen merupakan suatu ikatan kovalen nonpolar yang terjadi antara atom hidrogen dengan atom oksigen, nitrogen, atau fluorin. Ikatan ini sangat penting dalam banyak aspek kehidupan, mulai dari sifat air hingga kestabilan struktur molekul biologis.
 |
| Pengertian Ikatan Hidrogen: Senyawa, Contoh Soal |
Dalam artikel ini, kita akan membahas pengertian ikatan hidrogen secara lebih mendalam, senyawa yang terbentuk dari ikatan hidrogen, serta contoh soal yang berkaitan dengan ikatan hidrogen. Artikel ini terdiri dari 10 bagian yang akan membahas topik-topik berikut:
- Pengertian Ikatan Hidrogen
- Sifat Ikatan Hidrogen
- Bentuk Molekul dengan Ikatan Hidrogen
- Senyawa dengan Ikatan Hidrogen
- Ikatan Hidrogen dalam Air
- Ikatan Hidrogen dalam Molekul Biologis
- Keberadaan Ikatan Hidrogen di Alam
- Contoh Soal Ikatan Hidrogen
- Aplikasi Ikatan Hidrogen
- Kesimpulan
Pengertian Ikatan Hidrogen
Ikatan hidrogen terjadi ketika atom hidrogen membentuk suatu ikatan dengan atom lain yang memiliki elektronegativitas yang cukup tinggi, seperti oksigen, nitrogen, atau fluorin. Pada ikatan hidrogen, elektron yang dipakai untuk membentuk ikatan bersama-sama ditarik oleh kedua atom, sehingga terbentuk polaritas pada molekul.
Ikatan hidrogen biasanya terjadi pada molekul yang memiliki bentuk linier atau V-shaped, di mana kedua ujung molekul memiliki muatan yang berbeda. Ikatan ini sangat penting dalam berbagai aspek kehidupan, mulai dari sifat air hingga struktur molekul biologis.
Sifat Ikatan Hidrogen
Ikatan hidrogen memiliki beberapa sifat yang membedakannya dari jenis ikatan kovalen lainnya. Salah satu sifat ikatan hidrogen adalah kekuatannya yang relatif lemah dibandingkan dengan ikatan kovalen polar atau ikatan kovalen nonpolar. Namun, ikatan hidrogen ini cukup kuat untuk mempertahankan struktur molekul, seperti pada molekul DNA.
Selain itu, ikatan hidrogen juga memiliki sifat polar yang membuat molekul yang terbentuk dari ikatan hidrogen memiliki muatan parsial positif dan negatif di kedua ujung molekul. Sifat polar ini mempengaruhi sifat fisika dan kimia dari molekul tersebut, seperti titik didih, titik lebur, dan reaktivitas.
Bentuk Molekul dengan Ikatan Hidrogen
Bentuk molekul dengan ikatan hidrogen biasanya memiliki bentuk linier atau V-shaped. Contoh molekul dengan bentuk linier adalah molekul karbon dioksida (CO2), sedangkan molekul dengan bentuk V-shaped adalah molekul air (H2O). Bentuk molekul ini mempengaruhi sifat fisika dan kimia dari molekul tersebut, seperti titik didih, titik lebur, dan reaktivitas.
Jenis-Jenis Ikatan Hidrogen
Ikatan hidrogen dapat dibedakan menjadi dua jenis, yaitu ikatan hidrogen intermolekul dan ikatan hidrogen intramolekul.
Ikatan Hidrogen Intermolekul
Ikatan hidrogen intermolekul terjadi antara molekul-molekul yang berbeda, seperti antara molekul air. Ikatan ini bersifat relatif lemah dan mudah terputus, namun memiliki pengaruh yang signifikan pada sifat fisika dan kimia zat, seperti pada titik didih dan titik beku air.
Ikatan Hidrogen Intramolekul
Ikatan hidrogen intramolekul terjadi dalam satu molekul, seperti pada molekul asam salisilat yang memiliki ikatan hidrogen antara atom oksigen dan atom hidrogen pada gugus hidroksil. Ikatan hidrogen intramolekul ini mempengaruhi struktur dan sifat kimia dari molekul tersebut.
Kedua jenis ikatan hidrogen ini memiliki peran penting dalam berbagai aspek kehidupan, mulai dari sifat fisika dan kimia zat hingga struktur molekul biologis.
Ikatan Hidrogen di Makhluk Hidup
Ikatan hidrogen memiliki peran penting dalam makhluk hidup, terutama dalam struktur molekul biologis seperti DNA, protein, dan karbohidrat. Beberapa contoh peran ikatan hidrogen dalam makhluk hidup adalah:
Struktur DNA
Ikatan hidrogen antara pasangan basa pada rantai DNA membentuk struktur heliks ganda yang stabil. Pasangan basa adenin berikatan dengan timin melalui dua ikatan hidrogen, sedangkan pasangan basa guanin berikatan dengan sitosin melalui tiga ikatan hidrogen. Keberadaan ikatan hidrogen ini memungkinkan DNA untuk mempertahankan stabilitas strukturnya dan memainkan peran penting dalam pewarisan sifat.
Struktur protein
Ikatan hidrogen berperan dalam membentuk struktur sekunder dan tersier pada protein. Ikatan hidrogen antara gugus amida pada rantai polipeptida membentuk struktur heliks atau lembaran beta, sedangkan ikatan hidrogen antara rantai samping asam amino membentuk lipatan dan struktur tiga dimensi pada protein. Keberadaan ikatan hidrogen ini memungkinkan protein untuk mempertahankan struktur yang stabil dan memainkan peran penting dalam fungsi biologisnya.
Sifat air
Ikatan hidrogen pada molekul air memungkinkan air untuk memiliki sifat polar dan membentuk jaringan hidrogen yang kuat. Hal ini memungkinkan air untuk memainkan peran penting dalam berbagai proses biologis, seperti transportasi nutrisi, pembuangan limbah, dan regulasi suhu tubuh.
Struktur karbohidrat
Ikatan hidrogen antara gugus hidroksil pada monosakarida membentuk ikatan glikosidik yang membentuk polisakarida seperti selulosa dan amilum. Keberadaan ikatan hidrogen ini memungkinkan karbohidrat untuk membentuk struktur yang stabil dan memainkan peran penting dalam penyimpanan dan penggunaan energi dalam sel.
Dalam keseluruhan, ikatan hidrogen merupakan salah satu jenis ikatan yang penting dalam makhluk hidup dan memainkan peran penting dalam mempertahankan struktur dan fungsi biologis.
Senyawa dengan Ikatan Hidrogen
Beberapa senyawa yang terbentuk dari ikatan hidrogen antara lain air (H2O), amonia (NH3), asam klorida (HCl), dan asam asetat (CH3COOH). Senyawa-senyawa ini memiliki sifat-sifat yang khas, tergantung pada banyaknya ikatan hidrogen yang terbentuk pada molekul tersebut. Sebagai contoh, air memiliki dua ikatan hidrogen dan memiliki sifat-sifat seperti adhesi, koherensi, dan kapilaritas.
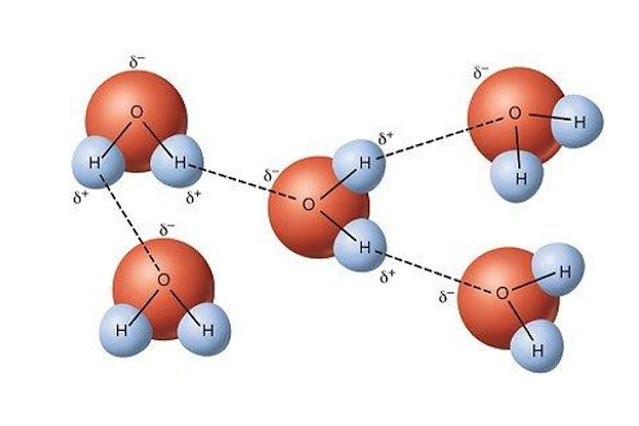
Ikatan Hidrogen dalam Air
Ikatan hidrogen dalam air sangat penting dalam menjelaskan sifat air, seperti adhesi, koherensi, dan kapilaritas. Ikatan hidrogen dalam air terjadi antara atom hidrogen pada satu molekul air dengan atom oksigen pada molekul air lainnya. Ikatan hidrogen ini membuat molekul air dapat saling melekat satu sama lain, sehingga tercipta fenomena adhesi dan koherensi.
Adhesi adalah kemampuan air untuk menempel pada permukaan benda, seperti pada dinding sel tumbuhan. Sementara itu, koherensi adalah kemampuan air untuk menempel pada dirinya sendiri, sehingga membentuk tetesan. Fenomena kapilaritas juga terjadi karena ikatan hidrogen dalam air, di mana air dapat naik ke atas pipa yang sangat sempit, seperti pada pembuluh tumbuhan.
Ikatan Hidrogen dalam Molekul Biologis
Ikatan hidrogen juga sangat penting dalam struktur molekul biologis, seperti pada DNA dan protein. Pada DNA, ikatan hidrogen membentuk pasangan basa antara adenin dan timin, serta guanin dan sitosin. Sedangkan pada protein, ikatan hidrogen membentuk struktur sekunder dan tersier dari protein, yang menentukan fungsi protein tersebut.
Keberadaan Ikatan Hidrogen di Alam
Di alam, ikatan hidrogen terdapat pada berbagai benda, mulai dari air hingga es. Es memiliki struktur kristal yang khas, di mana molekul air terikat satu sama lain melalui ikatan hidrogen, membentuk bentuk heksagonal. Ikatan hidrogen juga terdapat pada senyawa-senyawa organik, seperti alkohol dan asam karboksilat.
Contoh Soal Ikatan Hidrogen
- Jelaskan pengertian ikatan hidrogen beserta contohnya.
- Apa yang dimaksud dengan sifat polar pada ikatan hidrogen?
- Berikan contoh senyawa yang terbentuk dari ikatan hidrogen.
- Bagaimana ikatan hidrogen berperan dalam sifat air?
- Apa peran ikatan hidrogen dalam struktur molekul biologis?
- Apa yang dimaksud dengan kapilaritas dan bagaimana ikatan hidrogen berperan dalam fenomena ini?
- Bagaimana ikatan hidrogen terbentuk pada molekul?
- Apa yang dimaksud dengan bentuk molekul V-shaped?
- Apa yang dimaksud dengan struktur sekunder dan tersier dari protein?
- Apa yang dimaksud dengan struktur kristal es dan bagaimana ikatan hidrogen berperan dalam pembentukannya?
Jawaban
- Ikatan hidrogen adalah suatu ikatan kovalen nonpolar yang terjadi antara atom hidrogen dengan atom oksigen, nitrogen, atau fluorin. Contohnya adalah ikatan hidrogen antara molekul air, di mana atom hidrogen pada satu molekul terikat pada atom oksigen pada molekul lainnya.
- Sifat polar pada ikatan hidrogen terjadi karena perbedaan elektronegativitas antara atom hidrogen dan atom oksigen, nitrogen, atau fluorin. Hal ini menyebabkan muatan positif pada atom hidrogen dan muatan negatif pada atom lainnya, sehingga terbentuk polaritas pada molekul.
- Beberapa contoh senyawa yang terbentuk dari ikatan hidrogen adalah air (H2O), amonia (NH3), dan asam klorida (HCl).
- Ikatan hidrogen berperan dalam sifat air karena ikatan hidrogen pada molekul air memungkinkan adhesi, koherensi, dan kapilaritas pada air.
- Ikatan hidrogen berperan penting dalam struktur molekul biologis, seperti pada DNA dan protein. Pada DNA, ikatan hidrogen membentuk pasangan basa antara adenin dan timin, serta guanin dan sitosin. Sedangkan pada protein, ikatan hidrogen membentuk struktur sekunder dan tersier dari protein, yang menentukan fungsi protein tersebut.
- Kapilaritas adalah kemampuan suatu zat untuk naik atau turun melalui rongga-rongga kecil atau sumbu yang sangat sempit. Ikatan hidrogen berperan dalam fenomena ini karena ikatan hidrogen pada molekul air memungkinkan air untuk menempel pada dinding rongga atau pipa yang sangat sempit.
- Ikatan hidrogen terbentuk melalui interaksi elektrostatis antara atom hidrogen dan atom oksigen, nitrogen, atau fluorin. Atom hidrogen membentuk ikatan hidrogen dengan atom lainnya karena elektronnya tertarik oleh atom yang lebih elektronegatif.
- Bentuk molekul V-shaped merujuk pada bentuk molekul yang memiliki dua pasangan elektron bebas pada atom pusat dan dua atom lainnya terkait dengan atom pusat membentuk sudut sekitar 104,5 derajat, seperti pada molekul air.
- Struktur sekunder dan tersier dari protein merujuk pada bentuk tiga dimensi dari rantai polipeptida yang disusun oleh ikatan hidrogen antara rantai samping amino asam dan ikatan hidrogen antara rantai polipeptida itu sendiri.
- Struktur kristal es terbentuk karena ikatan hidrogen antara molekul air, di mana molekul air terikat satu sama lain membentuk bentuk heksagonal. Ikatan hidrogen juga memungkinkan es untuk memiliki densitas yang lebih rendah daripada air cair, sehingga es dapat mengapung di atas air.
Aplikasi Ikatan Hidrogen
Ikatan hidrogen memiliki banyak aplikasi dalam berbagai bidang, seperti dalam ilmu kimia, biologi, dan teknologi. Dalam ilmu kimia, ikatan hidrogen digunakan dalam penentuan struktur molekul dan reaksi kimia. Sedangkan dalam bidang biologi, ikatan hidrogen digunakan dalam pemahaman struktur dan fungsi protein serta DNA.
Dalam teknologi, ikatan hidrogen digunakan dalam berbagai aplikasi, seperti pada industri kosmetik, farmasi, dan bahan bakar. Dalam industri kosmetik, ikatan hidrogen digunakan dalam pembuatan sabun dan kosmetik lainnya. Sedangkan dalam industri farmasi, ikatan hidrogen digunakan dalam penentuan struktur molekul obat-obatan.
Kesimpulan
Ikatan hidrogen adalah suatu ikatan kovalen nonpolar yang terjadi antara atom hidrogen dengan atom oksigen, nitrogen, atau fluorin. Ikatan ini memiliki sifat-sifat yang khas, seperti kekuatan yang relatif lemah, sifat polar, dan pengaruh terhadap sifat fisika dan kimia dari molekul. Ikatan hidrogen sangat penting dalam berbagai aspek kehidupan, mulai dari sifat air hingga struktur molekul biologis.
Dalam artikel ini, kita telah membahas pengertian ikatan hidrogen secara lebih mendalam, senyawa yang terbentuk dari ikatan hidrogen, serta contoh soal yang berkaitan dengan ikatan hidrogen. Semoga artikel ini dapat membantu pembaca untuk memahami lebih dalam tentang ikatan hidrogen.
Sampai jumpa kembali di artikel menarik lainnya dari Bospedia!
FAQ
1. Apakah ikatan hidrogen lebih kuat daripada ikatan kovalen polar?
Ikatan hidrogen memiliki kekuatan yang relatif lemah dibandingkan dengan ikatan kovalen polar. Namun, ikatan hidrogen cukup kuat untuk mempertahankan struktur molekul, seperti pada molekul DNA. Oleh karena itu, tidak bisa dikatakan bahwa ikatan hidrogen lebih kuat atau lebih lemah daripada ikatan kovalen polar secara umum.
2. Apa yang terjadi jika ikatan hidrogen pada molekul DNA rusak?
Jika ikatan hidrogen pada molekul DNA rusak, dapat terjadi mutasi pada molekul tersebut yang dapat mempengaruhi fungsi dan karakteristik organisme yang mengandung molekul DNA tersebut.
3. Apakah semua senyawa yang mengandung atom hidrogen dapat membentuk ikatan hidrogen?
Tidak semua senyawa yang mengandung atom hidrogen dapat membentuk ikatan hidrogen. Ikatan hidrogen hanya terbentuk antara atom hidrogen dengan atom oksigen, nitrogen, atau fluorin yang memiliki elektronegativitas yang cukup tinggi.
4. Apa yang terjadi jika molekul air tidak memiliki ikatan hidrogen?
Jika molekul air tidak memiliki ikatan hidrogen, maka molekul tersebut tidak akan memiliki sifat polar dan tidak akan dapat saling melekat satu sama lain, sehingga tidak akan terbentuk sifat fisika dan kimia yang unik pada air, seperti adhesi, koherensi, dan kapilaritas.
5. Apakah ikatan hidrogen dapat terbentuk antara atom hidrogen dan atom lain selain oksigen, nitrogen, atau fluorin?
Ikatan hidrogen hanya dapat terbentuk antara atom hidrogen dan atom oksigen, nitrogen, atau fluorin yang memiliki elektronegativitas yang cukup tinggi. Atom lain yang memiliki elektronegativitas rendah, seperti karbon dan silikon, tidak dapat membentuk ikatan hidrogen.


Post a Comment